生命情報科学研究室
| 指導教員 | 諏訪牧子 教授 越中谷賢治 助教 |
|---|---|
| テーマ |
1.身体の全ての膜タンパク質情報をカタログ化 2.細胞膜表面を視覚化して全容を解明(ビジュアルプロテオミクス) 3.深層学習を用いた細胞の画像判別 4.創薬の重要ターゲットの機能発現メカニズムを理解し、予測 5.生命現象を予測し、制御 6.タンパク質が多様な機能を獲得してきた起源や変遷を解明 |
研究内容
近年、ゲノム配列情報やタンパク質立体構造、遺伝子発現情報など膨大な生命情報の電子データ(生物系ビッグデータ)が蓄積されています。
バイオインフォマティクスは、コンピューターを使って統計解析や機械学習などでこれら膨大な生命情報を網羅的に解読し、生命現象とどのような因果関係を持つかを分析する、最先端の分野です。本研究室ではこのバイオインフォマティクス手法により、膨大な生命情報を扱い生命の神秘を解き明かし、展開される生命現象のドラマの筋書き解明しょうとしています。
創薬ターゲットの膜タンパク質に特に注目し、それらの機能・構造、相互作用、さらに細胞内へのシグナル伝達パスウェイの理解を目指しています。解析ツールやデータベースを開発しつつ研究を進めています。実用面においては、新しい薬の開発への貢献が期待できます。
身体の全ての膜タンパク質情報をカタログ化する
ゲノム配列情報から得られる全膜タンパク質について、立体構造情報や機能情報を一元管理した総合DBを構築しています。さらに、膜タンパク質を起点とするシグナル伝達パスウェイのデータも蓄積しています。これらは研究室内の様々な解析の基盤になります。
細胞膜表面を視覚化して全容を解明する(ビジュアルプロテオミクス)
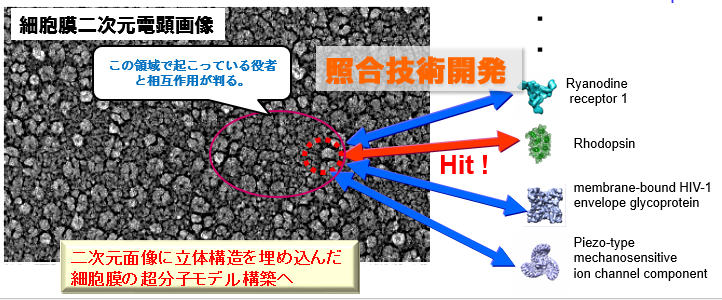
細胞表面の電顕画像上のタンパク質の画像全て対して立体構造情報を照合することでタンパク質の種類を同定する方法(左図)を研究しています。
実現できれば、例えば幹細胞の分化や、細胞内小胞の構造変化、疾患時の細胞の変化などの場面で、膜タンパク質同士の相互作用などを 直接捉えられるので、医薬品開発や再生医療等に貢献できる可能性があります。
深層学習を用いて細胞の画像を判別する

細胞は、周りの環境の違いにより、さまざまな形になります。つまり細胞の画像からその時の細胞の状態を知ることができるのです。しかし、細胞の状態と画像の相関性を一義的に人の目で見極めることは困難ですし、大量の画像の中からこれらを手作業で行うことはほとんど不可能です。
そこで、私たちは、深層学習(Deep learning)手法を用い、電子顕微鏡画像中の細胞を自動で検出・形状分類する技術を開発します。研究室では、様々な対象を扱っていますが、例えば、がん細胞と健常細胞の判別や、細胞内カルシウム濃度変化に伴う骨格筋小胞の構造変化判別などを行っています。図は、メラノーマのがん細胞が□枠で囲われて、正しく予測された例です。
創薬の重要ターゲットの機能発現メカニズムを理解し、予測する

Gタンパク質共役型受容体(GPCR)(右図)やカルシウムポンプなどの機能発現メカニズムを研究しています。配列解析、立体構造解析、分子動力学シミュレーションを用いて、リガンド分子と結合して構造変化し、細胞内にシグナルを伝達するまでの分子機構を探ります。
さらに、この機構からつながる細胞内シグナル伝達パスウェイを通じ、細胞核内で生じる生命現象(遺伝子発現など)まで予測できるデータベースシステムを作ろうとしています。
生命現象を予測し、制御する
例として匂い認識を取り上げます。匂い認識は、ヒトで数百種の匂い受容体が、匂い分子で活性化することから始まりますが、複数の匂い受容体の活性化パターンが記憶や感情と連動するため、におい分子による記憶、感情制御に繋がるかもしれません。様々な種類の匂い分子のブレンドに対する匂い受容体活性化のパターンを計算機上で予測する方法を研究しています。
タンパク質が多様な機能を獲得してきた起源や変遷を解明する
タンパク質の配列情報や立体構造情報を用いて、結合リガンドの特性、細胞内オルガネラなどへの局在位置、糖鎖などの化学修飾、ゲノム上の遺伝子座標、エクソン―イントロン構造など、様々な特性・属性などの相関性を、生物種間で全タンパク質レベルで詳細に追跡、比較して行きます。
研究者情報

| 教授:諏訪牧子 | |
| 学位 | 博士(理学) |
| 所属学会 | 日本バイオインフォマティクス学会、日本生物物理学会 |
| 研究分野 | バイオインフォマティクス、生物物理学、ゲノム情報科学、 タンパク質構造・機能科学 |

| 助教:越中谷賢治 | |
| 学位 | 博士(工学) |
| 所属学会 | 日本分子生物学会、日本農芸化学会 |
| 研究分野 | 分子生物学 |
